Впервые выявленный мНМРЛ без драйверных мутаций с высоким уровнем PD-L1
IMpower110*: монотерапия Атезолизумабом значительно увеличила выживаемость пациентов с высоким уровнем PD-L1 (TC ≥50% или IC ≥10%), независимо от гистологического типа рака1,2†
![Пациенты, ранее не получавшие химиотерапию, отобранные по уровню PD-L1 (≥1% опухолевых клеток [TC] или иммунных клеток [IC]), с неплоскоклеточным (nsq) или плоскоклеточным (sq) мНМРЛ (N=572).](https://oncohub.kz/wp-content/uploads/2024/12/scheme-1-patient-1-2-1.png)
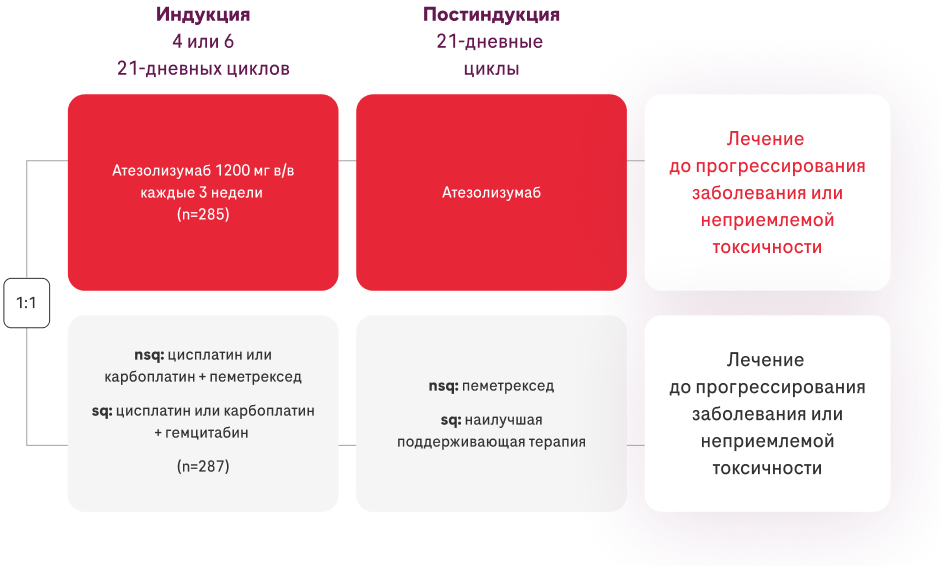
*IMpower110 — мультицентровое, международное, рандомизированное, открытое исследование III фазы1,2.
Монотерапия Атезолизумабом одобрена FDA в качестве терапии первой линии для пациентов с мНМРЛ с высоким уровнем PD-L1 без геномных опухолевых аберраций EGFR или ALK.
Основной конечной точкой была общая выживаемость (ОВ) в подгруппах, отобранных
по уровню PD-L1
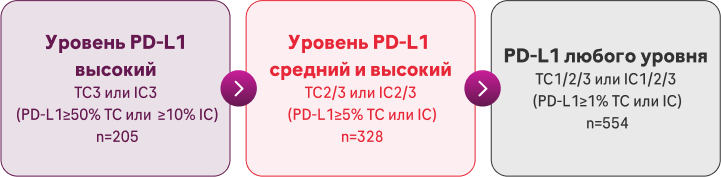


При промежуточном анализе у этих пациентов было выявлено статистически значимое преимущество в OВ при монотерапии Атезолизумабом по сравнению с химиотерапией.

Предустановленные границы общей выживаемости для этих подгрупп не были пересечены ни на момент промежуточного, ни на момент окончательного анализа.
Исходные характеристики пациентов с высокой экспрессией PD-L1 (TC ≥50% или IC ≥10%) в IMpower1101,2
| Характеристики пациентов | Атезолизумаб (n=107) | Химиотерапия на основе платины (n=98) |
Демография пациентов
| Возраст, медиана (диапазон), года | 63 (33-79) | 66 (33-87) |
| Возраст | 55,1 | 43,9 |
| Мужчины, % | 73,8 | 65,3 |
| Никогда не курили, % | 8,4 | 15,3 |
Раса, %
| Белая | 81,3 | 83,7 |
| Азиатская | 18,7 | 15,3 |
Гистология, %
| Неплоскоклеточный | 74,8 | 76,5 |
| Плоскоклеточный | 25,2 | 23,5 |
ECOG PS, %
| 0 | 32,7 | 38,8 |
| 1 | 67,3 | 61,2 |
Метастазы
| Метастазы в печени, % | 16,8 | 17,3 |
| Метастатические участки, медиана | 3 | 3 |
ECOG = Восточная кооперативная онкологическая группа; PS = статус работоспособности.
Общая выживаемость
Монотерапия Атезолизумабом привела к снижению риска смерти на 41% по сравнению с химиотерапией
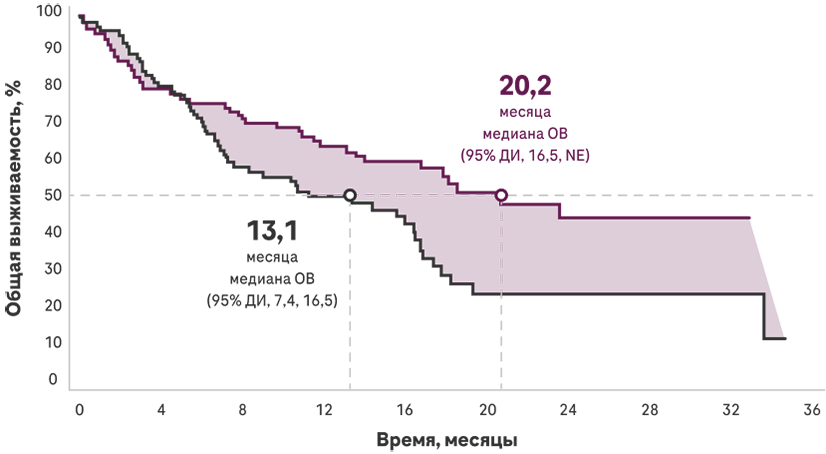

Число в группе риска
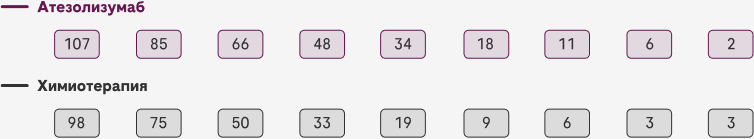
Медиана наблюдения у пациентов с высоким уровнем PD-L1 составила 15,7 месяцев
Почти две трети пациентов, получавших терапию Атезолизумабом, остались живы в течение 1 года: 12-месячная общая выживаемость у пациентов с высоким уровнем PD-L1 составила 64,9% при применении Атезолизумаба (95% ДИ, 55,4–74,4) по сравнению с 50,6% при химиотерапии на основе платины (95% ДИ, 40,0–61,3)

Ключевые анализы не были рассчитаны на демонстрацию статистически значимых различий.

Показатели общей выживаемости через 1 год были оценены с использованием методологии Каплана-Мейера для каждой группы лечения.
ВБП, УОО и ДО у пациентов с высоким уровнем PD-L11,2||
Медиана выживаемости без прогрессирования составила 8,1 месяца при терапии Атезолизумабом (95% ДИ, 6,8-11,0) против 5,0 месяцев при химиотерапии на основе платины (95% ДИ, 4,2-5,7) (КР=0,63‡; 95% ДИ, 0,45-0,88)

Уровень объективного ответа составил 38% с Атезолизумабом (95% ДИ, 29-48) против 29% с химиотерапией на основе платины (95% ДИ, 20-39)

Медиана длительности ответа не была достигнута с Атезолизумабом (95% ДИ, 11,8-NE) против 6,7 месяцев с химиотерапией на основе платины (95% ДИ, 5,5-17,3)
ALK = киназа анапластической лимфомы; EGFR = рецептор эпидермального фактора роста; ЦНС = центральная нервная система; ДИ = доверительный интервал;
КР = коэффициент риска; ITT = намерение лечить; WT = дикий тип; мНМРЛ = метастатический немелкоклеточный рак лёгких; nsq = неплоскоклеточный;
sq = плоскоклеточный; OВ = общая выживаемость; PD-L1 = лиганд запрограммированной клеточной смерти 1; ВБП = выживаемость без прогрессирования;
RECIST = критерии оценки ответа при солидных опухолях; TC = опухолевые клетки; IC = иммунные клетки, инфильтрирующие опухоль; УОО = уровень объективного ответа; ДО = длительность ответа; ПО = полный ответ; ЧО = частичный ответ; ECOG = Восточная кооперативная онкологическая группа;
PS = статус работоспособности; NE = не поддается оценке.
† На основе промежуточного анализа ОВ.
‡ Стратифицировано по полу и статусу эффективности ECOG.
§ На основе стратифицированного логрангового теста.
|| Как определено исследователем в соответствии с RECIST v1.1.
Источники
- ОХЛП Тецентрик, 1200 мг/20 мл. Приказ № N069768 от 07 декабря 2023 г.
- Rittmeyer A, Barlesi F, Waterkamp D, et al; OAK Study Group. Atezolizumab versus docetaxel in patients with previously treated non-small-cell lung cancer (OAK): a phase 3, open-label, multicentre randomised controlled trial. Lancet. 2017;389:255-265.
